Перейти к:
Сопоставление результатов иммунодиагностических тестов in vivo (проба Манту и проба с АТР) и in vitro (QuantiFERON – GIT) в группах детей, имеющих хроническую неспецифическую бронхолегочную патологию в сочетании с различными проявлениями туберкулезной инфекции
https://doi.org/10.34215/1609-1175-2022-4-25-29
Аннотация
Цель: подбор и сочетание иммунодиагностических тестов для выявления активного туберкулеза у детей, имеющих сопутствующую бронхолегочную патологию.
Материалы и методы. Нами проведено перспективное исследование детей и подростков (n = 236) с изолированным туберкулезом органов дыхания, с туберкулезом органов дыхания и наличием аллергических или инфекционно-воспалительных форм хронических неспецифических заболеваний легких (ХНЗЛ), с хроническими неспецифическими заболеваниями легких и достоверным отсутствием активного туберкулеза, но инфицированных микобактерией туберкулеза. Всем пациентам были проведены иммунодиагностические тесты: проба Манту, проба с аллергеном туберкулезным рекомбинантным (АТР), QuantiFERON – GIT.
Результаты. Установлено, что проба Манту и проба АТР обладают высокой чувствительностью как у детей с туберкулезом и сопутствующей патологией, так и без нее; у детей с сопутствующей туберкулезу бронхолегочной патологией результаты пробы Манту имеют некоторое отличие от результатов пробы у детей с изолированным туберкулезом. Проба Манту может быть положительной в результате многих других факторов кроме активной туберкулезной инфекции. А именно, аллергическая и инфекционно-воспалительная патологии легких оказывают влияние на результаты пробы Манту и у этой группы имеется тенденция к измененной чувствительности к тестам. В таком случае in vitro диагностика предпочтительнее, так как QuantiFERON-тест обладает высокой чувствительностью при туберкулезном процессе, независимо от наличия ХНЗЛ.
Заключение. Дети с ХНЗЛ инфекционно-воспалительного характера нуждаются в поэтапном обследовании с применением in vivo тестов и при необходимости in vitro. Детям с ХНЗЛ аллергического характера показано проведение теста in vitro уже на первом этапе.
Ключевые слова
Для цитирования:
Наконечная С.Л., Аксенова В.А., Мизерницкий Ю.Л. Сопоставление результатов иммунодиагностических тестов in vivo (проба Манту и проба с АТР) и in vitro (QuantiFERON – GIT) в группах детей, имеющих хроническую неспецифическую бронхолегочную патологию в сочетании с различными проявлениями туберкулезной инфекции. Тихоокеанский медицинский журнал. 2022;(4):25-29. https://doi.org/10.34215/1609-1175-2022-4-25-29
For citation:
Nakonechnaya S.L., Aksenova V.A., Mizernitskiy Yu.L. Comparative sensitivity of immunodiagnostic tests in vivo (Mantoux and RTA) and in vitro (QuantiFERON – GIT) in children with chronic nonspecific bronchopulmonary pathology associated with various tuberculosis. Pacific Medical Journal. 2022;(4):25-29. (In Russ.) https://doi.org/10.34215/1609-1175-2022-4-25-29
Определяющим компонентом стратегии ВОЗ по ликвидации туберкулеза является систематическое обследование лиц из групп высокого риска по туберкулезу. Одну из таких групп представляют собой дети с хроническими неспецифическими заболеваниями легких. В последние годы актуальным является подбор и сочетание иммунодиагностических тестов для выявления активного туберкулеза у детей, имеющих сопутствующую бронхолегочную патологию [1][2].
В течение ста лет основным методом раннего выявления туберкулеза у детей являлась массовая туберкулинодиагностика. Открытие антигенов, специфичных для Mycobacterium tuberculosis и отсутствующих в вакцинном штамме Mycobacterium bovis BCG, привело к разработке пробы с аллергеном туберкулезным рекомбинантным (АТР), лабораторных IGRA-тестов (анализ высвобождения гамма-интерферона, Interferon-Gamma Release Assays, интерферон гамма релиз ассейс). В литературе имеются данные, что внедрение пробы с аллергеном туберкулезным рекомбинантным в диагностическую практику позволяет эффективно выявлять пациентов с высоким риском развития туберкулеза [1]. На сегодня, по данным Global TB Report, IGRA-тесты рекомендованы для применения во всем мире [2], а именно QuantiFERON-TB Gold In-Tube является «золотым стандартом» из всех международно признанных эталонных стандартах на туберкулезную инфекцию из IGRA-тестов [3].
Однако, учитывая стоимость лабораторных тестов, они могут применяться только при наличии противопоказаний для проведения кожных иммунологических проб и в отдельных группах пациентов. Особую группу при диагностике туберкулеза представляют дети с аллергическими заболеваниями [4]. Аллергические состояния являются противопоказанием к постановке внутрикожных проб, поэтому требуют альтернативных методов диагностики туберкулеза [5].
Материалы и методы
Проведено открытое, простое, сплошное, сравнительное, многоцентровое исследование в период с 2019 по 2020 г. на базе стационара детско-подросткового отделения НМИЦ ФПИ и НИКИ педиатрии. Исследование было одобрено этическим комитетом. Для участия детей в исследовании от родителей или их законных представителей было получено добровольное информированное согласие (протокол № 81от 11.10.2019 г.).
Под нашим наблюдением находилось 236 детей и подростков в возрасте от 1 года до 17 лет. При анализе результатов иммунодиагностических тестов для выявления туберкулеза при сопутствующей неспецифической бронхолегочной патологии и без нее мы разделили детей на три подгруппы.
- Дети и подростки с туберкулезом органов дыхания и достоверным отсутствием ХНЗЛ – 93 человека (ТБ).
- Дети и подростки с туберкулезом органов дыхания и наличием различных форм ХНЗЛ – 65 человек (ТБ + ХНЗЛ).
- Дети и подростки с хроническими неспецифическими заболеваниями легких и достоверным отсутствием активного туберкулеза, но инфицированные микобактерией туберкулеза – 78 человек (ХНЗЛ).
Критериями включения являлись дети с хроническими неспецифическими заболеваниями легких и впервые выявленным активным туберкулезом органов. Критерием исключения являлось наличие у пациентов сопутствующих соматических заболеваний других органов и систем, осложняющих течение основного процесса в органах дыхания.
Всем пациентам проводили специфические иммунологические тесты: проба Манту, проба с АТР, QuantiFERON – GIT. Далее проводилось сравнение результатов этих тестов между собой в трех группах.
Статистическую значимость различий оценивали по критерию χ2. При сравнении результатов иммунодиагностических проб использовали критерий χ2 или точный критерий Фишера в зависимости от минимального предполагаемого числа. Различия считали достоверными при р < 0,05. Статистическую обработку материалов проводили с использованием пакета прикладных программ Microsoft Office 2016, IBM SPSS Statistics (26-я версия) и портала https://medstatistic.ru/.
Результаты исследования
Нами проведено сравнение результатов пробы Манту и пробы с АТР в группах ТБ и ТБ + ХНЗЛ.
В группе с диагнозом ТБ на пробу Манту положительные (89) и гиперергические (2) пробы реакции отмечены у 91 из обследованных детей ((97,8%) 95% ДИ [ 92,4–99,7]), сомнительные пробы отмечались у2 детей ((2,2%) 95% ДИ [ 0,2–7,6]). По результатам пробы с АТР положительные реакции получены у 90 обследованных детей ((96,8%) 95% ДИ [ 90,8–99,3]), отрицательные – у 3 ((3,2%) 95% ДИ [ 0,7–9,1]).
В группе с диагнозом ТБ + ХНЗЛ на пробу Манту сомнительный результат получен у 4 пациентов ((6,2%) 95% ДИ [ 1,7–15,0]), у 61 – результат положительный (60) и гиперергический (1) ((93,8%) 95% ДИ [ 85–98,3]). По результатам пробы с АТР положительные реакции получены у 59 обследованных пациентов ((90,8%) 95% ДИ [ 80,9–96,5]), отрицательные – у 6 ((9,2%) 95% ДИ [ 3,4–19,1]). Схематично это показано на рисунке 1.
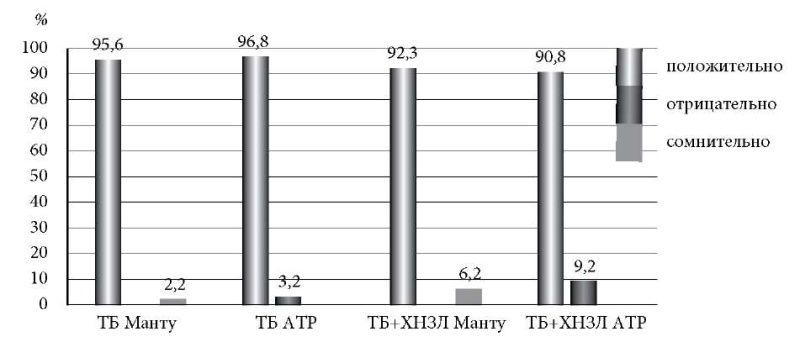
Рис. 1. Сравнение результатов пробы Манту и пробы с АТР у детей с ТБ и ТБ+ХНЗЛ. Описание в тексте.
Для изучения влияния бронхолегочной патологии на результат иммунодиагностики мы проанализировали результаты пробы Манту и пробы с АТР в группе детей с хроническими неспецифическими заболеваниями легких без туберкулеза, но инфицированных микобактерией туберкулеза (ХНЗЛ).
При сравнении данных иммунодиагностики у детей с ХНЗЛ без туберкулеза мы получили, что у 64 детей ((82%) 95% ДИ [ 71,7–89,8]) проба Манту положительная, у 14 сомнительная ((17,9%) 95% ДИ [ 10,2–28,3]), а на пробу с АТР только у 2 проба положительная ((2,6%) 95% ДИ [ 0,3–8,9]) а отрицательный результат получен у 76 пациентов ((97,4%) 95% ДИ [ 91,0–99,7]).
В группе детей с туберкулезом без сопутствующих заболеваний органов дыхания положительный результат QuantiFERON – GIT был отмечен у 87 пациентов ((93,5%) 95% ДИ [ 86,5–97,6]). В группе пациентов с туберкулезом и сочетанной хронической бронхолегочной патологией положительный результат QuantiFERON – GIT был у 56 пациентов ((86,1%) 95% ДИ [ 75,3–93,5]), а в группе детей с бронхолегочной патологией, но без туберкулеза результаты указанного теста были положительными у 4 пациентов ((5,1%) 95% ДИ [ 1,4–12,6]).
Таблица 1
Распределение пациентов по ответу на иммунологические пробы
ТБ, n = 93 | ТБ + ХНЗЛ,n = 65 | ХНЗЛ,n = 78 | χ2 | р | |
р. Манту + | 91 (97,8%) | 61 (93,8%) | 64 (82%) | 14,273 | 0,0008 |
АТР+ | 90 (96,8%) | 59 (90,8%) | 2 (2,6%) | 191,313 | 0,0 |
QuantiFERON+ | 87 (93,5%) | 56 (86,1%) | 4 (5,1%) | 162.941 | 0,0 |
Таблица 2
Чувствительность и специфичность иммунологических тестов
Чувствительность | Чувствительность при ХНЗЛ | Специфичность | |
п. Манту с 2ТЕ | 97,8% (95% ДИ [ 92,5–99,7]) | 93,8% (95% ДИ [ 84,9–98,3]) | 17,9% (95% ДИ [ 10,2–28,3]) |
АТР | 96,8% (95% ДИ [ 90,9–99,3]) | 90,8% (95% ДИ [ 91,0–99,7]) | 97,4% (95% ДИ [ 91,0–99,7]) |
QuantiFERON– GIT | 93,5% (95% ДИ [ 86,5–97,6]) | 86,1% (95% ДИ [ 75,3–93,5]) | 94,9% (95% ДИ [ 87,4–98,6]) |
Таблица 3
Результаты иммунологических тестов у детей с ХНЗЛ
р. Манту + | АТР+ | QuantiFERON– GIT+ | |
ХНЗЛ аллерг. (n =42) | 31 (70,7%) | 1 0,8% | 1 (2,4%) |
ХНЗЛ инф.-восп. (n = 36) | 33 (91,0%) | 1 1,6% | 3 (8,3%) |
Результаты анализов чувствительности и специфичности иммунологических тестов (табл. 2) показывают, что все три иммунологических теста обладают высокой чувствительностью как при отсутствии ХНЗЛ, так и при сочетании с туберкулезом. Однако при оценке специфичности отмечается низкие ее показатели при использовании п. Манту с 2ТЕ, в отличие от АТР и QuantiFERON – GIT, у которых специфичность находится на достаточно высоком уровне.
Для уточнения влияния неспецифической патологии на результаты иммунологических тестов in vitro и in vivo при наличии изменений, связанных с аллергической и инфекционно-воспалительной патологией, мы сравнили их в двух группах: ХНЗЛ аллер. (n = 42), ХНЗЛ инф.-восп. (n = 36). В результате анализа полученных данных показано, что положительный результат QuantiFERON – GIT+ в группе детей ХНЗЛ аллерг. без туберкулеза наблюдался у 1 пациента ((2,4%) 95% ДИ [ 0,06–12,5]), а в группе ХНЗЛ инф.-восп. у 3 пациентов ((8,3%) 95% ДИ [ 1,8–22,5]).
У 70,7% с аллергическим генезом выявлен положительный результат на пробу Манту, у детей с инфекционно-воспалительным генезом в 91,0% была положительная реакция. На пробу с АТР у детей с аллергическим генезом у 0,8% детей результат был положительный, у 1,6% детей с инфекционно-воспалительным генезом – положительный результат.
Из таблиц мы видим, что практически у всех детей результат на пробу Манту положительный. При этом у детей достоверно отсутствует активный туберкулез, что наглядно видно по результатам на пробу АТР. Полученные результаты были обоснованием для изучения тестов in vitro у этой группы пациентов.
Обсуждение полученных данных
Ранее полученые данные о том, что параметры оценки диагностической ценности пробы с АТР значительно выше, чем пробы Манту с 2 ТЕ. По данным Старшиновой А.А. и соавт. [6][7], прогностическая значимость положительного и отрицательного результатов кожных проб в развитии туберкулезной инфекции составила для пробы с АТР 82,1 и 85,0% соответственно (для пробы Манту 39,7 и 15,3%). Показатели диагностической значимости пробы с АТР и пробы Манту с 2 ТЕ в диагностике туберкулезной инфекции у подростков [8] составили 97,9 и 10,2% соответственно. Имеются данные о высокой частоте совпадений результатов проб с АТР и QfT [9], что, с одной стороны, подтверждает их достоверность, а с другой – свидетельствует о возможностях взаимной замены при необходимости. Впервые проведено сравнение in vivo и in vitro тестов у детей, имеющих бронхолегочную патологию. Нами установлено, что проба Манту и проба АТР обладает высокой чувствительностью как у детей с туберкулезоми сопутствующей патологией, так и без нее. Однако сомнительных результатов (6,2%) на пробу Манту и отрицательных результатов на пробу с АТР (9,2%) в группе с туберкулезом и сопутствующей патологией легких оказалось больше, чем в группе с изолированным туберкулезом, где сомнительных результатов на пробу Манту было 2,2% и отрицательных результатов на пробу с АТР 3,2%. Отсюда можно сделать вывод, что у детей с сопутствующей туберкулезу бронхолегочной патологией результаты пробы Манту имеют некоторое отличие от результатов пробы у детей с изолированным туберкулезом.
Проанализировав результаты пробы Манту в группе детей только с хроническими неспецифическими заболеваниями, но инфицированных МБТ, мы подтвердили ранее полученные данные, что проба Манту может быть положительной в результате многих других факторов, кроме активной туберкулезной инфекции. В нашем случае оказывает влияние аллергическая или инфекционно-воспалительная патология легких, которая приводит к искажению полученных результатов иммунодиагностики и соответственно к трудностям в диагностике туберкулеза. При этом сомнительные результаты значительно чаще встречается в группе с аллергопатологией, чем с инфекционно-воспалительным процессом (73,9% против 26,1%). Достоверность результата на пробу Манту невысокая по сравнению с пробой АТР. Это подтверждает, что аллергическая и инфекционно-воспалительная патологии легких оказывают влияние на результаты пробы Манту и у этой группы имеется тенденция к измененной чувствительности к тестам, что связано с тяжелой аллергической реакцией и снижением иммунного ответа. В таком случае in vitro диагностика предпочтительнее, так как QuantiFERON-тест обладает высокой чувствительностью притуберкулезном процессе, независимо от наличия ХНЗЛ.
Выводы
- Проба Манту и проба с АТР обладает высокой чувствительностью как у детей с туберкулезом и сопутствующей бронхолегочной патологией, так и без нее. Но специфичность пробы Манту в группе ХНЗЛ + ТБ ниже, чем специфичность пробы с АТР.
- QuantiFERON-тест обладает высокой чувствительностью при туберкулезном процессе, независимо от наличия ХНЗЛ. Также QuantiFERON-тест обладает высокой чувствительностью и специфичностью у детей инфицированных МБТ при наличии ХНЗЛ.
- Дети с ХНЗЛ инфекционно-воспалительного характера нуждаются в поэтапном обследовании с применением in vivo тестов и при необходимости in vitro. Детям с ХНЗЛ аллергического характера показано проведение теста in vitro уже на первом на первом этапе.
Конфликт интересов: авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Источник финансирования: авторы заявляют о финансировании проведенного исследования из собственных средств.
Список литературы
1. Кудлай Д.А., Старшинова А.А., Довгалюк И.Ф. Аллерген туберкулезный рекомбинантный: 10-летний опыт применения теста у детей и подростков в Российской Федерации (данные метаанализа). Педиатрия им. Г.Н. Сперанского. 2020;99(3):121–9. doi: 10.24110/0031-403X-202099-3-121-129
2. Всемирная организация здравоохранения. Глобальный отчет по туберкулезу. URL: https://apps.who.int/iris/bitstream/handle/10665/337538/9789240016095-eng.pdf
3. Maraisa B, Verkuijlb S, Casenghic M, Triasihd R. Paediatric tuberculosis – new advances to close persistent gaps. International Journal of Infectious Diseases. 2021;113(Supl. 1):63–7. doi: 10.1016/j.ijid.2021.02.003
4. Аксенова В.А. Туберкулез органов дыхания и хронические неспецифические заболевания легких / В кн.: Розинова Н.Н., Мизерницкий Ю.Л. (ред.). Хронические заболевания легких у детей. М.: Практика, 2011: 189–94.
5. Приказ Минздрава России от 29.12.2014 г. № 951 «Об утверждении методических рекомендаций по совершенствованию диагностики и лечения туберкулеза органов дыхания».
6. Яблонский П.К., Довгалюк И.Ф., Старшинова А.А., Якунова О.А. Значение современных иммунологических тестов в диагностике туберкулеза у детей. Клиническая иммунология. 2013;15(1):37–44. doi: 10.15789/1563-06252013-1-37-44
7. Старшинова А.А., Ананьев С.М., Овчинникова Ю.Э., Корнева Н.В., Довгалюк И.Ф. Результаты применения иммунологических тестов нового поколения у детей в условиях массовой вакцинации против туберкулеза. Туберкулез и болезни легких. 2017;95(5):46–52. doi: 10.21292/2075-1230-2017-95-5-46-52
8. Слогоцкая Л.В., Богородская Е.М., Сенчихина О.Ю., Никитина Г.В., Кудлай Д.А. Формирование групп риска заболевания туберкулезом при различных иммунологических методах обследования детского населения. Российский педиатрический журнал. 2017;4:207–13.
9. Белушков В.В., Лозовская М.Э., Новик Г.А., Гурина О.П., Шибакова Н.Д. Значение диаскинтеста и квантиферонового теста в диагностике туберкулеза у детей. Фундаментальные исследования. 2012;(7):34–9.
Об авторах
С. Л. НаконечнаяРоссия
Наконечная Софья Левановна – аспирант
127473, Москва, ул. Достоевского, 4, корп. 2
В. А. Аксенова
Россия
Москва
Ю. Л. Мизерницкий
Россия
Москва
Рецензия
Для цитирования:
Наконечная С.Л., Аксенова В.А., Мизерницкий Ю.Л. Сопоставление результатов иммунодиагностических тестов in vivo (проба Манту и проба с АТР) и in vitro (QuantiFERON – GIT) в группах детей, имеющих хроническую неспецифическую бронхолегочную патологию в сочетании с различными проявлениями туберкулезной инфекции. Тихоокеанский медицинский журнал. 2022;(4):25-29. https://doi.org/10.34215/1609-1175-2022-4-25-29
For citation:
Nakonechnaya S.L., Aksenova V.A., Mizernitskiy Yu.L. Comparative sensitivity of immunodiagnostic tests in vivo (Mantoux and RTA) and in vitro (QuantiFERON – GIT) in children with chronic nonspecific bronchopulmonary pathology associated with various tuberculosis. Pacific Medical Journal. 2022;(4):25-29. (In Russ.) https://doi.org/10.34215/1609-1175-2022-4-25-29





































