Перейти к:
Опыт и перспективы внедрения информационных технологий в программу медицинской реабилитации пациентов с нарушениями мозгового кровообращения
https://doi.org/10.34215/1609-1175-2024-1-53-59
Аннотация
Цель: оценка реабилитационного потенциала пациентов с нарушением мозгового кровообращения для проспективного наблюдения и эффективной медицинской реабилитации. Материалы и методы. Обследованы пациенты с цереброваскулярными заболеваниями (n = 20) и перенесенным острым нарушением мозгового кровообращения (n = 22), составившие основную группу. Проведена интегральная оценка состояния здоровья с применением диагностического комплекса «Дермограф компьютерный для топической диагностики очагов патологии внутренних органов» (ДгКТД-01). Изучены показатели исходного уровня, проведен сравнительный анализ основной группы и группы контроля (n = 10). Пациентам основной группы проведена коррекция состояния здоровья на «Аппарат-корректоре компьютеризованного воздействия низкоинтенсивным электромагнитным полем для нормализации функциональной активности центральной и периферической нервной системы» (АНКФ-01) курсом из 10 сессий еженедельно с предварительной функционально-топической диагностикой на комплексе ДгКТД-01. Результаты. У пациентов, перенесших острое нарушение мозгового кровообращения, происходит функциональная перестройка вегетативной регуляции с большей выраженностью активации симпатического звена, у пациентов с цереброваскулярными заболеваниями – парасимпатического. Определяющим фактором при нарушении мозгового кровообращения являются показатели базовых функций F2 и F3. Выделена модель прогнозирования вероятности развития острых повторных нарушений мозгового кровообращения, определены дополнительные диагностические критерии для дифференциальной диагностики. Целенаправленное изменение потенциалов возбуждения (торможения) в корково-подкорковых взаимоотношениях меняет вегетативный баланс, стимулирует микроциркуляцию, мышечно-тоническую функцию, нейротрофическую регуляцию. Эти влияния стабилизируют и улучшают состояние пациентов. Эффективность реабилитационных мероприятий с применением АНКФ-01 выше у пациентов после перенесенного нарушения острого мозгового кровообращения. Заключение. Пациенты с нарушением мозгового кровообращения имеют специфические особенности адаптационных возможностей организма, что указывает на существование дифференциации в формировании функционального статуса организма с учетом особенностей заболевания, индивидуальных ресурсов и компенсаторных возможностей. Реабилитация на основе применения АНКФ-01 повышает эффективность мероприятий, направленных на предупреждение органических изменений головного мозга, и позволяет существенно улучшить прогнозы и снизить процент инвалидизации этой категории пациентов.
Ключевые слова
Для цитирования:
Меркулова Г.А., Пегова Е.В., Ришко Е.Ю., Крыжановский С.П. Опыт и перспективы внедрения информационных технологий в программу медицинской реабилитации пациентов с нарушениями мозгового кровообращения. Тихоокеанский медицинский журнал. 2024;(1):53-59. https://doi.org/10.34215/1609-1175-2024-1-53-59
For citation:
Merkulova G.A., Pegova E.V., Rishko E.Yu., Kryzhanovsky S.P. Experience and prospects of introducing information technologies in the program of medical rehabilitation of patients with cerebral circulation disorders. Pacific Medical Journal. 2024;(1):53-59. (In Russ.) https://doi.org/10.34215/1609-1175-2024-1-53-59
Инсульт и хроническая ишемия головного мозга занимают ведущее положение среди причин общей смертности, инвалидности, потребности в длительных реабилитационных мероприятиях [1]. Это обусловлено многообразием последствий поражений центральной нервной системы (ЦНС), реабилитационным потенциалом и тяжестью сопутствующих соматических заболеваний [2]. Особую актуальность представляют разработка и внедрение новых эффективных технологий в области цереброваскулярной патологии для совершенствования системы оценки реабилитационного потенциала и расширения возможностей медицинской реабилитации с целью повышения качества медицинской помощи и ее экономической эффективности. Реабилитационные программы должны быть комплексными и включать применение медикаментозных и немедикаментозных методов стимуляции восстановительного процесса [3].
Результаты исследований активирующей (неспецифической) системы мозга в естественной (тонической) активности вегетативной нервной системы легли в основу разработки новой технологии информационной (функционально-топической) диагностики и коррекции дисфункций организма [4]. Был разработан комплекс с расширенной функцией, который сочетает диагностическую (дермограф компьютерный для регистрации и анализа топографии сопротивления кожи постоянному сверхслабому стабилизированному току для топической диагностики очагов патологии внутренних органов человека – ДгКТД-01) [5] и оздоровительную (аппарат-корректор компьютеризованного воздействия низкоинтенсивным электромагнитным полем для нормализации функциональной активности центральной и периферической нервной системы – АНКФ-01) [6] системы. Технология составляет мониторинг индивидуального здоровья как замкнутый цикл: пациент – диагностика состояний и выявление выраженных дисфункций – коррекция дисфункций – контроль. Диагностическая ценность технологии доказана в клинических исследованиях и не вызывает сомнений [7–9].
Цель исследования: оценка реабилитационного потенциала пациентов с нарушением мозгового кровообращения для проспективного наблюдения и эффективной медицинской реабилитации.
Материалы и методы
Проведено контролируемое проспективное открытое исследование на базе ФГБУЗ МО ДВО РАН совместно с НИЦ «Арктика» ДВО РАН. Исследование одобрено этическим комитетом МО ДВО РАН (Протокол № 27 от 18.06.2020 г.).
В исследовании участвовали 42 пациента в возрасте 47–79 лет. Их разделяли на 2 основные группы с учетом возраста и общего состояния. Критерии включения в группу – пациенты с нарушением мозгового кровообращения (НМК).
Первую основную группу (n = 22, средний возраст 74,2 ± 2,5 года) составили пациенты, перенесшие острое нарушение мозгового кровообращения (ОНМК) в раннем восстановительном периоде, во вторую основную группу (n = 20, средний возраст 64,2 ± 3,9 года) вошли пациенты с цереброваскулярными заболеваниями (церебральный атеросклероз, церебральный атеросклероз с гипертензией). В исследование не включали пациентов с обострением соматического заболевания и не способных полностью понять информацию о процедуре исследования. Контрольную группу (n = 10, средний возраст 61,2 ± 1,7 года) составили 10 условно здоровых добровольцев.
На начальном этапе исследования проводили регистрацию исходных показателей, сравнение выборок обследуемых с применением ДгКТД-01. Методика обследования основана на использовании компьютерной системы дермографии и заключается в сканировании электрофизиологических параметров (электрического сопротивления) микрозон кожи ушной раковины по специально разработанным маршрутам, записанным в память персонального компьютера. Процедура не имеет противопоказаний, неинвазивна и безболезненна [10]. При проведении исследований определены количественные интегральные показатели, характеризующие функциональное состояние обследуемых: вегетативный индекс (ВИ), иммунный статус (ИС), индекс здоровья (ИЗ), группа диспансеризации (ГД) [11]. Признаки формирования патологической доминанты определялись при системном анализе графиков базовых функций (F), отображающих локальный сегментарный вегетативный тонус различных рецепторов внутренних органов. Мы исследовали значения F1–F4, которые соответствуют уровню тонической активности адренорецепторов. F1 отражает состояние мышечных рецепторов, F2 – стенки артериол, F3 – рецепторов венозного звена микроциркуляторного русла, F4 – адренорецепторов соединительной ткани и нервной системы. Выраженность показателей устанавливалась относительно их средних величин в проекции сегментов головы С*8–1 (в соответствии с принципами висцеро-соматической интеграции С*6–8 – лобная и лицевая, С*3–5 – височно-теменная, С*1–2 затылочная области) и шейного отдела позвоночника С1–7. Обращали внимание на отклонение амплитуды графика от средней линии: отклонение кривой вверх характеризует усиление тонуса в сторону ваготонии, вниз – в сторону симпатикотонии.
На следующем этапе по результатам обследования проведена коррекция выявленных дисфункций пациентов основной группы на АНКФ-01. Работа прибора основана на воздействии (экспозиции) на центральную и периферическую нервные системы низкоинтенсивными электромагнитными и инфракрасными полями строго заданных частот диапазона ритмической активности головного мозга. Такая экспозиция целенаправленно устраняет очаги патологически усиленного возбуждения (торможения) в отдельно взятом отделе нервной системы путем перераспределения активности неспецифической системы мозга по различным каналам управления вегетативной нервной системы (симпатическая – парасимпатическая). Поля создаются центральным и внешними излучателями, форма и частота, время и последовательность экспозиций излучателей управляются специальной программой с персонального компьютера. Процедура не требует специальной подготовки, выполняется в положении сидя или полулежа на спине, в состоянии покоя с установкой излучателей (стационарные и внешние). Стационарные излучатели, выполненные в виде наушников, надеваются на голову обследуемого, внешние излучатели устанавливаются в область остистых отростков 6–7-го шейных позвонков [12]. В наших исследованиях коррекцию проводили курсом, состоящим из 10 сессий. Проведено сравнение данных после окончания реабилитации. Все обследуемые дали добровольное информированное согласие на участие в исследовании.
Статистическую обработку результатов исследования проводили на персональном компьютере в операционных средах Windows XP с помощью приложения Microsoft Excel. При выполнении расчетов использовали пакет прикладных программ «Статистика 6.0». Для каждого вариационного ряда полученных результатов исследования вычисляли средние арифметические величины (М), средние квадратические отклонения (σ), относительные величины (Р), ошибки средних арифметических и относительных величин (m). При осуществлении сравнительного анализа изученных показателей применяли t-критерий Стьюдента. Нулевая гипотеза о различиях между признаками анализируемых выборок принималась при р ≤ 0,05.
Результаты исследования
В контрольной группе количественные интегральные показатели ВИ (3,8 ± 0,2), ИЗ (3,8 ± 0,3), ИС (0,6 ± 0,03) находились в диапазоне референсных величин, соответствуя нормотоническому типу вегетативного регулирования ЦНС, сбалансированному состоянию эрготропных и трофотропных влияний практически здоровых лиц с нормальным развитием, сохраненным состоянием иммунной систем. Значения коэффициента ВИ в группе 1 были существенно (р ≤ 0,05) выше (5,4 ± 0,3), а в группе 2 – ниже (2,5 ± 0,4), чем в контрольной группе. Общая направленность вегетативных изменений в группе 1 симпатикотоническая, в группе 2 преобладает ваготоническая.
Среди пациентов, перенесших ОНМК в раннем восстановительном периоде, лиц с симпатикотонией было в 2,7 раза больше, чем в группе 2, при отсутствии таковых в контрольной группе (41 и 15% соответственно). В группе 2 пациентов больше в 1,6 раза лиц с ваготонией, чем в группе 1 и контроле (32, 50, 18% соответственно). Отметим, что значения ВИ с высокой степенью коррелирует (r ≥ 0,5) с показателем ИЗ. Степень напряжения регулирующих процессов вегетативного обеспечения отразилась в значениях показателя ИЗ основных группах – был существенно выше (5,4 ± 0,3 и 4,7 ± 0,2), чем в контрольной группе. Учитывая, что значения ИЗ соотносятся с показателями ГД (более высокое значение группы отражает худшие параметры здоровья), присутствует большое количество лиц с высокой вероятностью наличия заболеваний в стадии компенсации и субкомпенсации. По классификации функциональных состояний в группе 1 лиц 4ГД больше в 2,7 раза, чем в группе 2, при отсутствии таковых в контроле (41 и 15% соответственно). Различия установлены и по значениям показателя ИС, который был существенно ниже в группе 1 (0,3 ± 0,02), в группе 2 составил 0,4 ± 0,03. Отметим, что его значения менее 0,5 ед. характеризуют в целом сниженные функциональные характеристики иммунной системы.
В контрольной группе в зоне сегментов С*8–1 и С1–7 графики базовых функций не имели разнонаправленных, однонаправленных максимумов или минимумов, были синхронны между собой: F1’ расположена между F2 и F3, F1 и F2 не пересекалась с F3; рассогласование между F2 и F3 составило не более 1,5 отн. ед. Базовая функция F1 находилась в доверительном интервале 1,0–2,0 усл. ед. (1,3 ± 0,04), F2 – 0,5–1,5 (1,0 ± 0,04), F3 – 1,5–2,3 (1,5 ± 0,03), F4 – 1,0–2,0 (1,5 ± 0,03), что указывает на адекватный уровень регуляции центральными структурами мозга сосудистого тонуса, обеспечивая оптимальный кровоток и нейротрофическую регуляцию.
В основных группах выявлены и определены сегментарное представительство, суммарные максимальные отклонения базовых функций и достоверные различия показателей (p ≤ 0,05) относительно контрольной группы. Выражались в группе 1 в зоне сегментов С*8–6 экстремумом амплитудных показателей при максимальных значениях F1 (2,2 ± 0,02), F2 (1,8 ± 0,03) и минимальных F3 (1,4 ± 0,02); в С*5–3 максимальных F1 (2,4 ± 0,02), F2 (2,8 ± 0,03) и F4 (2,3 ± 0,03); в C*2–1 выражались экстремумом амплитудных показателей при максимальных F2 (1,9 ± 0,03) и F4 (2,0 ± 0,03), в C1–7 – максимальных F2 (1,8 ± 0,03) и F4 (2,9 ± 0,03) (рис. 1).
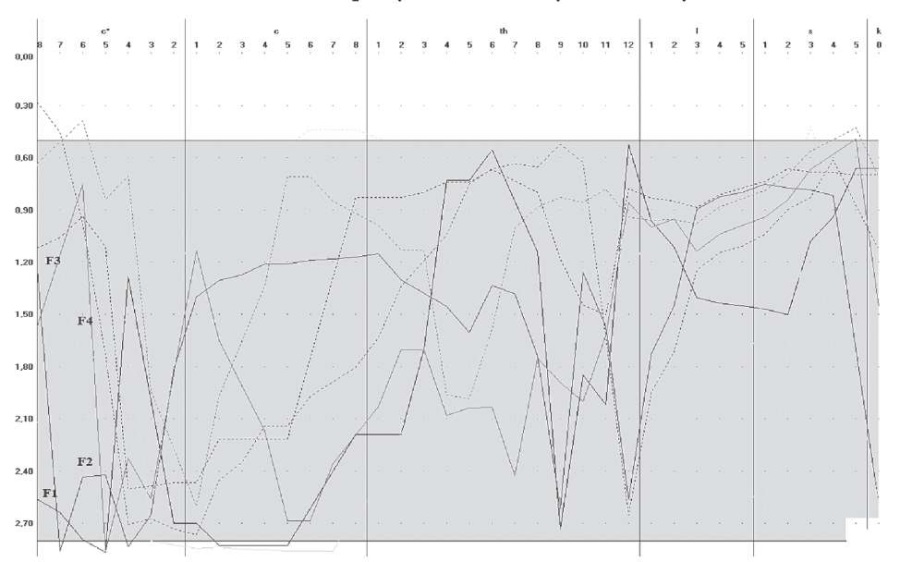
Рис. 1. Амплитудно-конфигурационный вид графиков
базовых функций в зоне сегментов С*8–1 и С1–7
у пациента перенесшего острое нарушение мозгового кровообращения.
Суммарные максимальные отклонения базовых функций и достоверные различия (p ≤ 0,05) показателей относительно контроля в группе 2 выражались в зоне сегментов С*8–6 экстремумом амплитудных показателей при минимальных значениях F1 (0,4 ± 0,01), F2 (0,5 ± 0,01) и максимальных F3 (2,5 ± 0,02); в С*2–1 – максимальных F4 (2,0 ± 0,02), в C1–7 максимальных F2 (1,9 ± 0,03) и F4 (2,5 ± 0,02) (рис. 2).

Рис. 2. Амплитудно-конфигурационный вид графиков
базовых функций F1, F2, F3, F4 в зоне сегментов С*8–1 и С1–7
у пациента с церебральной гипертензией.
Выявлены особенности в группах с НМК, заключающиеся в статистически достоверном (p ≤ 0,05) отличии показателей в зоне сегментов С*8–6, где в группе 1 значения функции F1 и F2 были значимо выше, чем в группе 2 (2,2 ± 0,02 и 0,4 ± 0,01; 1,8 ± 0,03 и 0,5 ± 0,01 соответственно), а F3 ниже (1,4 ± 0,02 и 2,5 ± 0,2 соответственно). В зоне сегментов С*5–3 в группе 1 значения функции F1 и F2 были значимо выше F1 (2,4 ± 0,02 и 1,4 ± 0,03; 2,8 ± 0,03 и 0,8 ± 0,04 и соответственно). Определены сегментарное представительство, достоверные различия показателей (p ≤ 0,05) базовых функций, которые позволили выделить дополнительные диагностические критерии, характеризующие изучаемые состояния при НМК. К ним относятся в группе 1 в зоне сегментов С*8–3 экстремум амплитудных показателей при максимальных значениях F1, F2 и минимальных F3. В основной группе 2 – в зоне сегментов С*8–6 экстремум амплитудных показателей при минимальных значениях F1, F2 и максимальных F3, в С*5–3 при максимальных значениях F2 (когда F2 > F3). Следует подчеркнуть, что в основных группах отсутствовали значимые различия в зоне сегментов С*2–1, С1–7 по значениям F2, F4, однако значительно превышали референсные границы (от 2,0 до 2,9 усл. ед.).
После окончания курса реабилитации отмечалось уравновешивание механизмов вегетативной регуляции – статистически значимое (p ≤ 0,05) снижение в группе 1 показателя ВИ до 4,7 ± 0,3, в группе 2 повышение до 3,8 ± 0,3. Изменилось соотношение обследуемых по вегетативному регулированию – в группе 1 снижение в 2,2 раза лиц с симпатикотонией (до 18%), увеличение с нормотонией (до 46%) и ваготонией (до 36%). В группе 2 – снижение в 1,4 раза лиц с ваготонией (до 35%), увеличение в 2,6 раза с нормотонией (до 65%). Кроме того, в группе 1 показатель ИЗ вошел в диапазон нормы (4,5 ± 0,2). По классификации функциональных состояний отмечено снижение в 2,5 раза лиц с 4ГД (до 23%), увеличение в 1,3 раза с 3ГД (до 77%). В группе 2 изменения по значениям ИЗ были статистически незначимы, при этом отмечено увеличение в 1,1 раза лиц 3ГД (до 75%) и 2ГД (до 25%) за счет отсутствия лиц с 4ГД. Показатели ИС в основных группах улучшились, однако оставались ниже границы нормативных значений (0,4 ± 0,02).
С точки зрения прогностического потенциала в группе 1 в зоне сегментов С*8–1 отмечена достаточно выраженная тенденция снижения к значениям референтных границ показателя F1, F2, когда значения F2 стали меньше F3. Кроме того изменения произошли в сегментах С*2–1 и С1–7 со снижением преобладающего исходного тонуса F4. В группе 2 отмечена тенденция F1-F4 к значениям референтных границ в сегментах C*8–6 и показателей F4 в С*5–1 (табл.).
Таблица
Динамика показателей базовых функций
после реабилитации с применением аппарат-корректора АНКФ-01
Группа | Базовая функция | Сегменты | |||
С*8–6 до после реабилитации | С*5–3 до после реабилитации | С* 2–1 до после реабилитации | С1–7 до после реабилитации | ||
1 | F1 | 2,2 ± 0,02 1,0 ± 0,04* | 2,4 ± 0,02 1,5 ± 0,03* | 1,7 ± 0,02 1,1 ± 0,03* | 1,8 ± 0,03 1,0 ± 0,03* |
F2 | 1,8 ± 0,03 1,2 ± 0,03* | 2,8 ± 0,03 1,6 ± 0,02* | 1,9 ± 0,03 1,2 ± 0,02* | 1,8 ± 0,03 1,2 ± 0,04 | |
F3 | 1,4 ± 0,02 1,8 ± 0,02 | 1,7 ± 0,02 1,9 ± 0,03 | 1,7 ± 0,03 1,6 ± 0,03 | 1,4 ± 0,04 1,8 ± 0,03 | |
F4 | 1,4 ± 0,03 1,3 ± 0,04 | 2,3 ± 0,03 1,6 ± 0,02* | 2,0 ± 0,03 1,6 ± 0,04 | 2,9 ± 0,03 1,5 ± 0,04* | |
2 | F1 | 0,4 ± 0,01 1,2 ± 0,02* | 1,8 ± 0,03 2,0 ± 0,02 | 1,9 ± 0,03 1,7 ± 0,03 | 1,4 ± 0,04 1,2 ± 0,03 |
F2 | 0,5 ± 0,0 1,2 ± 0,03* | 1,1 ± 0,03 1,5 ± 0,02 | 1,3 ± 0,02 1,6 ± 0,04 | 1,9 ± 0,03 1,2 ± 0,03* | |
F3 | 2,5 ± 0,02 1,6 ± 0,02* | 1,9 ± 0,02 2,0 ± 0,03 | 1,8 ± 0,03 1,5 ± 0,03 | 1,9 ± 0,03 1,6 ± 0,02 | |
F4 | 1,2 ± 0,03 1,9 ± 0,02* | 1,7 ± 0,03 1,9 ± 0,02* | 2,0 ± 0,02 1,2 ± 0,03* | 2,5 ± 0,02 1,9 ± 0,03 | |
Примечание: * – достоверные различия по сравнению со значением показателя
в группе до реабилитации (p < 0,05).
Обсуждение полученных данных
Наши исследования показали, что для пациентов с нарушениями мозгового кровообращения характерна дифференциация в формировании функционального статуса организма с учетом особенностей заболевания, индивидуальных ресурсов и компенсаторных возможностей организма. У пациентов после перенесенного ОНМК в раннем восстановительном периоде изменение вегетативного баланса определяется симпатической составляющей, что соотносится, вероятно, с более негативным клиническим статусом пациентов. У пациентов с цереброваскулярными заболеваниями проявляется ваготоническая направленность изменений. Это состояние может быть связано с более «спокойным» функционированием систем и умеренной активацией высших контуров управления, а также свидетельствует об истощении функциональных резервов организма. Полученные нами данные сопоставимы с результатами других исследований [13]. Показатели ИС в группах с НМК были сходными и характеризовались как недостаточность активности иммунной системы.
В результате проведенного исследования определены максимальные отклонения базовых функций и достоверные различия (p ≤ 0,05) показателей относительно контрольной группы, что позволило выделить сегментарную область, ведущее звено, выраженность функциональных нарушений у пациентов основных групп. Определяющим фактором при нарушении мозгового кровообращения явились показатели базовых функций F2 и F3. У пациентов после перенесенного ОНМК в зоне сегментов С*8–3 показатели указывают на дерегуляцию нейротрофических процессов, характеризующиеся нарушением гемодинамики в микроциркуляторном звене церебральной сосудистой трассы с явлениями вазоконстрикторных реакций, дисциркуляции в венозном русле. У пациентов с цереброваскулярными заболеваниями в зоне сегментов С*8–5 свидетельствуют о нарушении венозного компонента церебральной гемодинамики, а в С*5–3 – и о повышенном тонусе артериальных сосудов. Доминирование значений F2 над F3 указывает на преобладание стенозирующего процесса с явлениями ишемии сосудистого бассейна, что повышает риск ишемического повреждения [14]. Следует подчеркнуть, что в основных группах в зоне сегментов С*2–1, С1–7 отсутствовали значимые различия по значениям F2, F4, однако значительно превышали референсные границы, что указывает на нарушения локального вегетативного тонуса, наличие сформировавшейся патологической системы и отражает нейротрофические процессы в шейном отделе позвоночника.
Определены сегментарное представительство, достоверные различия показателей (p ≤ 0,05) базовых функций, которые позволили выделить дополнительные диагностические критерии, характеризующие изучаемые состояния при НМК. К ним относятся в группе 1 в зоне сегментов С*8–3 экстремум амплитудных показателей при максимальных значениях F1, F2 и минимальных F3, которые следует представлять как модель прогнозирования вероятности развития острых повторных нарушений мозгового кровообращения являются прогностической моделью выявления лиц развития ОНМК. В основной группе 2 – в зоне сегментов С*8–6 экстремум амплитудных показателей при минимальных значениях F1, F2 и максимальных F3, в С*5–3 при максимальных значениях F2 (когда F2 > F3).
Эффективность применения аппарат корректора АНКФ-01 в программе медицинской реабилитации показана статистически достоверными изменениями вегетативного компонента за счет уменьшения симпатического влияния на регуляторные процессы, повышения функциональных возможностей организма и изменения локального сегментарного вегетативного тонуса различных групп рецепторов. Активность последних в первой группе характеризуется достоверным снижением (p ≤ 0,05) в С*8–1 показателя F1, в С*5–1 – F2 и F3 (при этом значения F2 стали меньше значений F3), а в С*2–1 и С1–7 – F1, F4. Тогда как в основной группе 2 по окончании периода исследования значимое снижение (р ≤ 0,05) показателей от исходного уровня зафиксировано в зоне сегментов С*8–6 функций F1–F4, в С*5–3 – F4, значения F2 выходили за референсный диапазон. Данные изменения оцениваются как признаки снижения мышечно-тонического напряжения, относительной компенсации церебральной гемодинамики и улучшения нейротрофической регуляции.
Таким образом, пациенты основной группы 1 имеют более высокие возможности восстановления статуса на следующих этапах реабилитации, а пациенты группы 2 – более низкий резерв адаптации.
Заключение
Пациенты с нарушением мозгового кровообращения имеют специфические особенности адаптационных возможностей организма, что указывает на существование дифференциации в формировании функционального статуса организма с учетом особенностей заболевания, индивидуальных ресурсов и компенсаторных возможностей организма. Реабилитация на основе применения АНКФ-01 будет способствовать повышению эффективности мероприятий, направленных на предупреждение преждевременного формирования выраженных органических изменений головного мозга, что позволит существенно улучшить прогнозы и снизить процент инвалидизации этой категории пациентов.
Конфликт интересов: авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Источник финансирования: работа выполнена в рамках государственного задания Министерства образования и науки Российской Федерации, субсидия из федерального бюджета № 075-03-2022-724/2.
Список литературы
1. Мачинский П.А., Плотникова Н.А., Ульянкин В.Е., Кемайкин С.П., Рыбаков А.Г. Сравнительная характеристика показателей смертности и летальности от ишемического и геморрагического инсультов в России. Известия высших учебных заведений. Поволжский регион. Медицинские науки. 2019;2(50):112–32. doi: 10.21685/2072-3032-2019-2-11
2. Golubnitschaja O, Potuznik P, Polivka J Jr, Pesta M, Kaverina O, Pieper CC, Kropp M, Thumann G, Erb C, Karabatsiakis A, Stetkarova I, Polivka J, Costigliola V. Ischemic stroke of unclear aetiology: a case-by-case analysis and call for a multi-professional predictive, preventive and personalised approach. EPMA J. 2022; 13(4):535–45. doi: 10.1007/s13167-022-00307-z
3. Кадыков А.С., Шахпаронова Н.В. Реабилитация после инсульта. М.: ООО Медицинское информационное агентство, 2017. 240 с.
4. Шабанов Г.А., Максимов А.Л., Рыбченко А.А. Функционально-топическая диагностика организма человека на основе анализа ритмической активности головного мозга. Владивосток: Дальнаука, 2011. 206 с.
5. Лебедев Ю.А., Шабанов Г.А., Рыбченко А.А. Дермограф компьютерный для топической диагностики очагов патологии внутренних органов человека. Медицинская техника. 2007;5:37–9.
6. Рыбченко А.А., Лебедев Ю.А., Шабанов Г.А., Короченцев В.И. Программно-аппаратный комплекс для коррекции выраженных дисфункций внутренних органов человека на основе анализа ритмической активности головного мозга. Медицинская техника. 2010;1:27–9
7. Опыт и перспективы использования компьютерных и информационных технологий в диагностике и профилактике донозологических состояний и заболеваний / Под ред. А.А. Шепарева, А.Л. Максимова. Владивосток: Медицина ДВ, 2017. 6–39 с.
8. Меркулова Г.А., Пегова Е.В. Новые методические подходы в системе ранней диагностики мастопатии с применением метода компьютерной дермографии. Казанский медицинский журнал. 2019;1:117–24. doi: 10.17816/KMJ2019-117
9. Меркулова Г.А., Пегова Е.В. Использование принципов донозологической диагностики для оценки функционального состояния организма детского контингента в условиях Севера. Человек на Севере: системные механизмы адаптации: сборник трудов, посвященный 90-летию основания Магадана / под ред. Н.Н. Беседновой. Магадан: Экспрессполиграфия, 2019. 160–172 с.
10. Методика регистрации и анализа данных по оценке индивидуального здоровья с помощью диагностического комплекса ДгКТД-01. Уч. метод. пособие. А.А. Рыбченко, Г.А. Шабанов, Е.В. Пегова, Г.А. Меркулова. Владивосток: Издво Дальневост. ун-та, 2009. 96 с.
11. Шепарев А.А., Меркулова Г.А., Пегова Е.В., Сивочалова О.В. Диагностика нарушений репродуктивной функции мужчин с применением компьютерной технологии ДгКТД-01. Акушерство и гинекология. 2015;3:87–93.
12. Рыбченко А.А., Шабанов Г.А., Пегова Е.В., Меркулова Г.А. Аппарат корректор для нормализации функциональной активности центральной и периферической нервной системы АНКФ-01 «Лучезар». Пособие для врачей. Владивосток. 2013. 94 с.
13. Берлогина С.Ю., Герасимова Л.И. Вегетативная регуляция в системе кровообращения у лиц в раннем восстановительном периоде ишемического гемодинамического инсульта. Фундаментальные исследования. 2011;10-3:477–80.
14. Бокерия Л.А., Бузиашвили Ю.И., Шумилина М.В. Нарушения церебрального венозного кровообращения у больных с сердечно-сосудистой патологией (головная боль, ишемия, атеросклероз). Москва, 2003. 162 с.
Об авторах
Г. А. МеркуловаРоссия
Меркулова Галина Анатольевна – канд. мед. наук, научный сотрудник
685000, г. Магадан, ул. Карла Маркса, 24 тел.: +7 (950) 299-85-79
Е. В. Пегова
Россия
Магадан
Е. Ю. Ришко
Россия
Владивосток
С. П. Крыжановский
Россия
Владивосток
Рецензия
Для цитирования:
Меркулова Г.А., Пегова Е.В., Ришко Е.Ю., Крыжановский С.П. Опыт и перспективы внедрения информационных технологий в программу медицинской реабилитации пациентов с нарушениями мозгового кровообращения. Тихоокеанский медицинский журнал. 2024;(1):53-59. https://doi.org/10.34215/1609-1175-2024-1-53-59
For citation:
Merkulova G.A., Pegova E.V., Rishko E.Yu., Kryzhanovsky S.P. Experience and prospects of introducing information technologies in the program of medical rehabilitation of patients with cerebral circulation disorders. Pacific Medical Journal. 2024;(1):53-59. (In Russ.) https://doi.org/10.34215/1609-1175-2024-1-53-59





































