Перейти к:
Опыт применения продленной вено-венозной гемодиафильтрации в интенсивной терапии пациентов с тяжелой термической травмой
https://doi.org/10.34215/1609-1175-2025-2-86-91
Аннотация
Ожоговая болезнь в стадии острой ожоговой токсемии представляет собой симптомокомплекс взаимосвязанных и взаимоутяжеляющих друг друга патологических состояний, объединить которые уместно в синдром взаимного отягощения. Это прежде всего синдром системной воспалительной реакции, характеризующийся тяжелым эндотоксикозом, иммунной депрессией и гиперметаболическим синдромом. Одним из основных направлений многокомпонентного лечения тяжелой термической травмы является проведение полноценной детоксикационной терапии, позволяющее предотвратить развитие осложнений ожоговой болезни и улучшить прогноз течения заболевания. Применение процедур гемодиафильтрации у пациентов в стадии ожоговой токсемии ведет к значительному улучшению гемодинамики, оксигенирующей функции легких и корригирует патологические изменения гомеостаза. Полученные данные демонстрируют новые возможности интенсивной терапии у пациентов с глубокими ожогами, и включение в протокол лечения гемодиафильтрации позволит уменьшить летальность и сокращение времени стационарного лечения
Для цитирования:
Грибань П.А., Майстровский К.В., Усов В.В., Оробий О.Е., Полежаев А.А., Обыденникова Т.Н., Терехов С.М., Костива Е.Е. Опыт применения продленной вено-венозной гемодиафильтрации в интенсивной терапии пациентов с тяжелой термической травмой. Тихоокеанский медицинский журнал. 2025;(2):86-91. https://doi.org/10.34215/1609-1175-2025-2-86-91
For citation:
Griban P.A., Maystrovskiy K.V., Usov V.V., Orobiy O.E., Polezhaev A.A., Obydennikova T.N., Terehov S.M., Kostiva E.E. Application of prolonged veno-venous hemodiafiltration in intensive care for patients with severe thermal injuries. Pacific Medical Journal. 2025;(2):86-91. (In Russ.) https://doi.org/10.34215/1609-1175-2025-2-86-91
Проблема лечения термических ожогов продолжает оставаться актуальной, что связано не только с частотой их получения в быту, на производстве, в условиях катастроф мирного и военного времени, но и с утяжелением течения ожоговой болезни. В России ежегодно ожоги получают 130 000 – 160 000 человек, из которых около 50 тысяч госпитализируется в специализированные хирургические отделения с целью необходимости комплексного лечения [1–3]. Сложной категорией пострадавших являются пациенты с глубокими и обширными термическими поражениями – свыше 50 процентов поверхности тела – с развитием тяжелой ожоговой болезни [4][5]. При этом быстро развиваются эндотоксикоз и септикотоксемия, которые ведут к выраженной полиорганной недостаточности и значительно отягощают общее состояние пациента и ухудшают прогноз [6]. Летальность у пострадавших данной категории даже в специализированных отделениях, технически оснащенных, с возможностью применения современных методов лечения остается достаточно высокой и достигает 50% [1][7][8].
В настоящей работе обобщен опыт лечения 8 пациентов (5 мужчин, 3 женщины) с глубокими и обширными термическими поражениями свыше 50 процентов поверхности тела, которые находились на стационарном лечении в ожоговом отделении Дальневосточного окружного медицинского центра (ДВОМЦ) города Владивостока в 2023–2024 гг. Тяжесть состояния пациентов оценивали с помощью индекса Франка при котором учитывается площадь глубоких ожогов, и значения свыше 90 свидетельствуют о неблагоприятном прогнозе. В наших случаях этот показатель был на уровне 116,5 (92; 140), что прогностически явно свидетельствовало о потенциально неблагоприятном исходе ожоговой травмы у данных пациентов.
Все пострадавшие доставлены в ожоговое отделение из региональных медицинских организаций Приморского края. В краевых лечебных учреждениях им проводилась экстренная противошоковая терапия, выполнялась телемедицинская консультация врачом-реаниматологом и комбустиологом. Во время консультации оценивалась возможность эвакуации пострадавшего в ожоговое отделение ДВОМЦ различными видами транспорта. Через 48–72 часа с момента травмы тяжелообожженные были транспортированы в специализированное отделение бригадами территориального Центра медицины катастроф. У троих пострадавших этиологическим фактором ожогов было пламя при пожаре, у других пациентов – горячая вода.
В связи с обширным и глубоким поражением кожных покровов у поступивших пациентов развивалась выраженная ожоговая болезнь, проявляющаяся на начальном этапе синдромом системной воспалительной реакции, который вызывается выбросом провоспалительных цитокинов в ответ на травму [9][10]. В последующем по мере восстановления микроциркуляции в зоне термического поражения происходит массивное выделение в системный кровоток продуктов распада обожженных тканей и большого количества биологически активных соединений. Также выраженное влияние оказывает развивающийся парез желудочно-кишечного тракта и увеличение проницаемости кишечной стенки, что приводит к дополнительной резорбционной интоксикации [11, 12]. При позднем удалении некротических тканей происходит усугубление данных процессов, в последующем возникает синдром встречного противовоспалительного ответа, что приводит к иммунной дизрегуляции. Одновременно в зоне термического поражения происходит активное развитие местной хирургической инфекции, что на фоне снижения иммунной защиты часто приводит к генерализации процесса с исходов в сепсис. Системная воспалительная реакция, тяжелый эндотоксикоз, иммунная дизрегуляция и нарастающие катаболические процессы приводят к быстрому развитию полиорганной недостаточности, что значительно отягощает состояние пострадавших.
Таким образом, длительное наличие массива омерт-вевших покровных тканей в зоне термического воздействия является очередным ключевым фактором развития ожоговой болезни. Патогенетическое лечение в данный период состоит из двух основных взаимодополняющих компонентов: активной хирургической тактики, включающей раннее удаление некротического струпа с закрытием раневой поверхности и мощной дезинтоксикационной терапии. Выполнение оперативного иссечения омертвевших покровных тканей у пациентов с обширными поражениями – это достаточно продолжительный многоэтапный процесс, сопровождающийся различными осложнениями местного и системного характера. В связи с этим проведение эффективной дезинтоксикационной терапии у данной категории пациентов требует современных высокотехнологичных методов, которые позволяют длительно корригировать патологические изменения гомеостаза. В этой связи дезинтоксикационная терапия приобретает ведущее значение и включение в комплекс гемодиафильтрации существенно повышает ее эффективность.
В отделении реанимации и интенсивной терапии (ОРИТ) ожогового отделении ДВОМЦ мы применяли экстракорпоральные методы детоксикации аппаратом Asahi PlasAuto Sigma в режиме предиллюции с использованием гемофильтра UltraFlux Emic2. Антикоагулянтная терапия проводилась гепарином под контролем АЧТВ, скорость кровотока 180 ± 30 мл/мин, скорость потока субституата 40 мл/кг/час. Длительность процедуры составляла от 16 до 32 часов. Пяти пациентам сеанс гемодиафильтрации проводился дважды, а одному пострадавшему было проведено 3 процедуры. Всего было проведено 15 экстракорпоральных процедур. Ни в одном случае нами не отмечено осложнений, связанных с лечебной процедурой: тромбирования экстракорпорального контура, развития тяжелой печеночной недостаточности, профузного кровотечения, нарушения сердечной деятельности, пирогенных и аллергических реакций.
У пострадавших после проведения процедур гемодиафильтрации наблюдалось улучшение гемодинамики, оксигенирующей функции легких, ментального статуса, а также изменение тяжести состояния по шкале SOFA. Клинические показатели подтверждались лабораторными данными: купировалась нарастающая гипернатриемия и ацидоз, снижался уровень провоспалительных маркеров (табл. 1).
Данные результаты свидетельствуют об эффективности проводимой последовательной продленной вено-венозной гемодиафильтрации, что говорит о ее положительном, целенаправленном влиянии на патогенез ожоговой болезни. Проведение процедур экстракорпоральной аппаратной детоксикации позволило нам купировать развивающиеся явления токсемии и септикотоксемии, предотвратить развитие возможных осложнений ожоговой болезни, в том числе и полиорганной недостаточности, а также максимально быстро приступить к хирургическим процедурам: некрэктомии и восстановлению поврежденных кожных покровов с применением различных методов дермато пластики. При этом были отмечены лучшие результаты приживления кожных трансплантатов и, соответственно, более раннее функциональное восстановление пациентов.
Таблица 1
Контроль клинических и лабораторных параметров у пациентов до и после проведения процедуры продленной вено-венозной гемодиафильтрации (CVVHDF)
Клинико-лабораторные показатели | Показатели перед началом сеанса CVVHDF | Через 36 часов | Через 72 часа |
САД (мм. рт. ст.) | 62 ± 2,8 | 75 ± 2,6 | 82 ± 3,4 |
SOFA | 7 баллов | 6 баллов | 5 баллов |
pH | 7,26 ± 0,03 | 7,33 ± 0,02 | 7,35 ± 0,03 |
Na+ | 152 ± 4,6 ммоль/л | 144 ± 2,8 ммоль/л | 137 ± 3,1 ммоль/л |
К+ | 4,4 ± 0,4 ммоль/л | 4,2 ± 0,3 ммоль/л | 4.1 ± 0,4 ммоль/л |
Lactate | 1,7 ± 0,2 ммоль/л | 1,3 ± 0,2 ммоль/л | 0.8 ± 0,1 ммоль/л |
CRP | 5,6 ± 4,6 мг/л | 4,5 ± 3,2 мг/л | 32 ± 2,7 мг/л |
PCT | > 2 нг/л | 2 ± 0,5 нг/л | < 0,5 нг/мл |
РаО2 / FiО2 | 236 ± 12,5 | 270 ± 20,4 | 312 ± 16,2 |
РаCО2 | 42,4 ± 1,0 мм рт. ст. | 40,1 ± 0,8 мм рт. ст. | 42,2 ± 1,2 мм рт. ст. |
Клинический случай
Пациент М., 39 лет, находился на стационарном лечении в ожоговом отделении ФГБУЗ «ДВОМЦ ФМБА России» с 20.09.2024 г. по 07.12.2024 г. с диагнозом: Термический ожог пламенем (18.09.24) головы, шеи, туловища, левой верхней конечности и нижних конечностей II–III степени 65% поверхности тела. Ожог верхних дыхательных путей I степени. Ожоговая болезнь, острая ожоговая токсемия. ИФ – 140 единиц. Прогноз для жизни пациента при поступлении – неблагоприятный.
Обстоятельства травмы. Со слов пострадавшего, около 12.00 18.09.2024 г. он получил обширные термические ожоги пламенем в результате взрыва горючей воздушно-пылевой взвеси на промышленном предприятии. Бригадой скорой медицинской помощи был доставлен в Спасскую городскую больницу (Приморский край), где проводились неотложные противошоковые мероприятия, выполнялась первичная хирургическая обработка ран, декомпрессионная некротомия. В первые сутки после травмы проведена телемедицинская консультация со специалистами ожогового отделения, в ходе которой была определена дальнейшая тактика лечения пострадавшего. 20.09.2024 г. авиатранспортом пациент был доставлен в специализированное отделение ДВОМЦ.
Общее состояние пациента при поступлении крайне тяжелое, заторможен, положение с ограничением, температура тела 37,8 °С. Пострадавший правильного телосложения, удовлетворительного питания. Носовое дыхание свободное, аускультативно в легких дыхание жестковатое, частота дыхательных движений – 22 в минуту. Тоны сердца громкие, ритмичные, пульс – 96 ударов в минуту, язык сухой, розовый, живот участвует в акте дыхания, симметричный, при пальпации безболезненный. Диурез на фоне проводимой инфузионной терапии снижен.
Местный статус. В области головы, шеи, передней поверхности туловища, левой верхней ожоговые раны бледно-розового цвета, лишенные эпидермиса, в области задней поверхности туловища и нижних конечностей ожоговые раны представлены некротическим струпом темно-серого цвета. Определяется выраженное циркулярное сдавление мягких тканей в области пораженных бедер и голеней.
Тяжесть состояния пострадавшего подтверждалась лабораторными показателями: клинический анализ крови при поступлении – лейкоциты 18,6 × 109, эритроциты – 3,76 × 1012, гемоглобин – 118 г/л, гематокрит – 44,3%, тромбоциты – 238; биохимический анализ крови при поступлении – креатинин – 112 мкмоль/л, альбумин – 23,6 г/л, билирубин общий – 14,2 мкмоль/л, глюкоза – 7,56 ммоль/л, амилаза – 12 Ед/л, белок общий – 48,8 г/л, мочевина – 7,4 ммоль/л, АЛТ – 22,4 Ед/л, АСТ – 34 Ед/л; индекс Франка – 116.
При поступлении в специализированное отделение пострадавшему в условиях операционной была выполнена хирургическая обработка ран, в ходе которой окончательно установлена площадь и глубина термического поражения, также выполнена дополнительная некротомия глубоких ран в области бедер и голеней. После выполнения оперативного пособия пациент был помещен в ОРИТ на специализированную флюидизирующую кровать, где была продолжена интенсивная поликомпонентная терапия, включающая оптимальную инфузионно-трансфузионную терапию, рациональную антибактериальную терапию, пролонгированную респираторную поддержку, сбалансированную нутриционную поддержку в соответствии с клиническими рекомендациями.
Несмотря на проводимую активную хирургическую тактику лечения, большая площадь термического поражения не позволила быстро и одномоментно убрать весь массив омертвевших покровных тканей. Несмотря на ранние сроки начала оперативного лечения, у пациента развилась выраженная ожоговая болезнь, так как удаление некротического струпа выполнялось в несколько этапов. С целью купирования проявлений острой ожоговой токсемии и последующей септикотоксемии нами выполнялось 2 процедуры продленной вено-венозной гемодиафильтрации на аппарате Asahi PlasAuto Sigma в режиме предиллюции с использованием гемофильтра UltraFlux Emic2 (рис. 1). Венозный доступ для проведения процедуры осуществлен через v. femoralis dextra, катетеризация осуществлялась под УЗИ-контролем. Длительность сеансов гемодиафильтрации составляла 28 и 32 часа соответственно.
Проведенные в ходе лечения пациенту процедуры экстракорпоральной детоксикации позволили нам не только эффективно купировать явления ожоговой болезни, но и максимально быстро выполнить следующие травматичные оперативные вмешательства.
– 3-и сутки после травмы – хирургическая обработка ожоговых ран, некротомия в области ран обоих бедер и голеней.
– 6-е сутки после травмы – хирургическая обработка ожоговых ран, эпифасциальная некрэктомия ожогового струпа в области бедер и голеней.
– 7–8-е сутки после травмы – процедура продленной вено-венозной гемодиафильтрации.
– 11-е сутки после травмы – хирургическая обработка ожоговых ран, эпифасциальная и тангенциальная некрэктомия ожогового струпа в области туловища, аутодермопластика ран нижних конечностей (рис. 2).
– 14–15-е сутки после травмы – процедура продленной вено-венозной гемодиафильтрации.
– 17-е сутки после травмы – хирургическая обработка ожоговых ран, некрэктомия, аутодермопластика ран туловища.
– 28-е сутки после травмы – аутодермопластика ран нижних конечностей.
– 41-е сутки после травмы – аутодермопластика ран туловища и нижних конечностей.
– 53-е сутки после травмы – аутодермопластика остаточных рассеянных ран нижних конечностей.
Пациенту также регулярно проводили санации ожоговых ран растворами антисептиков, накладывали повязки с различными раневыми покрытиями и мазями. После стабилизации состояния и оперативного укрытия большей части ожоговых ран пострадавшему выполняли ранние реабилитационные мероприятия, включающие лечебную физкультуру, физиотерапевтическое лечение, психологическую поддержку.
Проведенное нами активное оперативное лечение глубоких ожоговых ран и методы экстракорпоральной детоксикации, использованные в комплексной интенсивной терапии пострадавшего, позволили получить хороший клинический результат. Спустя 2 месяца после травмы пациент был выписан из стационара на амбулаторное долечивание с небольшими рассеянными ранами до 1% поверхности тела. Ожоговое отделение пострадавший покинул самостоятельно, опираясь на трость (рис. 3). Через месяц после выписки из стационара пациент был консультирован специалистами ожогового отделения. Реконвалесценту с целью реабилитации назначены курсы физиотерапевтического лечения и лечебной физкультуры.
Пациенты с тяжелой ожоговой травмой нуждаются в активной хирургической тактике лечения и высокотехнологичной интенсивной терапии в условиях специализированных отделений. От своевременности и качества оказания помощи в период острой ожоговой токсемии в значительной степени зависят как исход термической травмы, так и сроки стационарного лечения. На основании данных клинических случаев можно сказать, что применение высокотехнологичной аппаратной вено-венозной гемодиафильтрации, применяемой параллельно с активной хирургической тактикой, существенно улучшило результаты лечения проявлений ожоговой болезни, способствовало предупреждению тяжелых полиорганных нарушений и сократило сроки пластического закрытия ран. Основным принципом проведения экстракорпоральной детоксикации в ОРИТ ожогового отделения являлось раннее начало процедуры аппаратной гемодиафильтрации до развития органных дисфункций, что позволяло предотвратить тяжелые осложнения, улучшить прогноз и сократить сроки лечения пациентов.
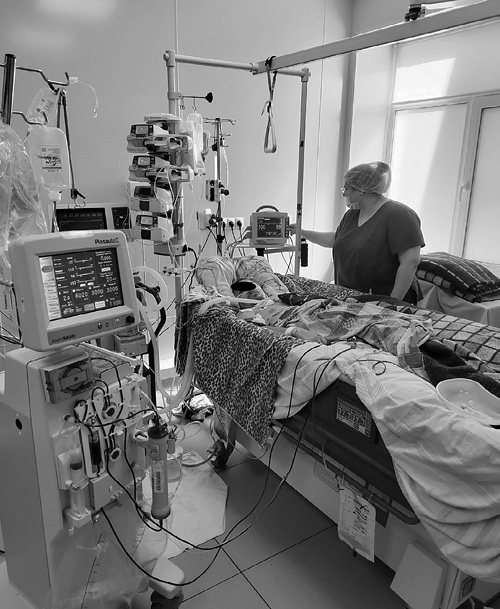
Рис. 1. Пациент М., 39 лет. Процедура продленной вено-венозной гемодиафильтрации. 7-е сутки после травмы.
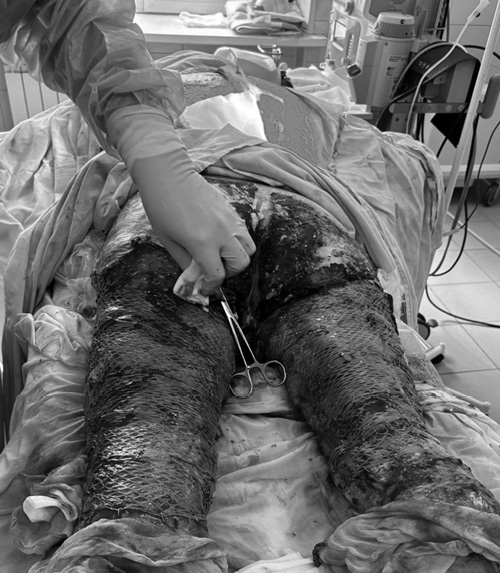
Рис. 2. Пациент М., 39 лет. Хирургическая обработка ожоговых ран, аутодермопластика ран нижних конечностей. 11-е сутки после травмы.
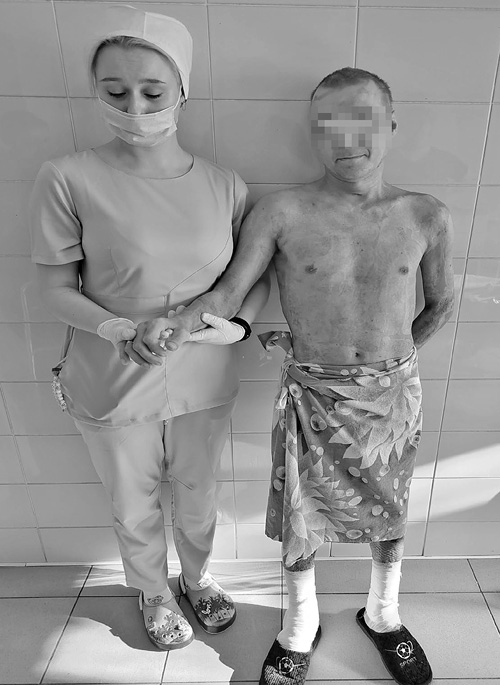
Рис. 3. Пациент М., 39 лет. День выписки из ожогового отделения.
Заключение
Несмотря на применение активной хирургической тактики лечения, у пациентов с обширными термическими поражениями свыше 50 процентов поверхности тела развивается выраженная ожоговая болезнь, проявляющаяся синдромом системной воспалительной реакции, тяжелым эндотоксикозом, иммунной дизрегуляцией. Прогрессирующее развитие каскада патологических процессов при ожоговой болезни приводит к быстрому развитию полиорганной недостаточности, что значительно ухудшает прогноз у данной категории пациентов. Важную роль в успешном лечении пострадавших с критическими ожогами играет наличие эффективной дезинтоксикационной терапии, включающей современные высокотехнологичные аппаратные методы. Включение в лечение пациентов с ожоговой болезнью процедур продленной вено-венозной гемодиафильтрации в программу интенсивной терапии тяжелообожженных имеет положительные перспективы при условии детальной отработки методики проведения процедуры и достаточном ресурсном обеспечении лечебного учреждения.
Список литературы
1. Алексеев А.А., Бобровников А.Э., Малютина Н.Б., Филимонов К.А. Анализ и особенности работы ожоговых стационаров Российской Федерации в 2022 году. Комбустиология. 2023;69–70.
2. Peck MD, Toppi JT. Epidemiology and Prevention of Burns Throughout the World. In: Jeschke MG, Kamolz L-P, Sjöberg F, Wolf SE, editors. Handbook of burns. Voume.1. Cham, Springer. 2020;17-57.
3. Burn Incidence and Treatment in the United States: 2016. American Burn Association. 2017. URL: http://ameriburn.org/who-we-are/media/burn-incidence-fact-sheet/ (Accessed Feb 02, 2025)
4. Зиновьев Е.В., Мануковский В.А., Заворотний О.О., Костяков Д.В. Анализ особенностей течения ожоговой травмы с учетом величины индекса тяжести поражений. Неотложная хирургия им. ИИ Джанелидзе, 2023;1(10):32–9.
5. Грибань П.А., Терехов С.М., Майстровский К.В., Усов В.В., Полежаев А.А., Протопопов В.В., Сотниченко С.А., Богданов В.А. Опыт лечения пострадавших с критической термической травмой в ожоговом отделении Дальневосточного окружного медицинского центра ФМБА России. Тихоокеанский медицинский журнал. 2023;2:89– 93.
6. Преснякова М.В., Арефьев И.Ю., Галова Е.А., Крестова Е.И., Костина О.В. Значимость биологических маркеров эндотелиопатии при развитии «раннего» сепсиса у тяжелообожженных. Клиническая лабораторная диагностика. 2024;69 (6):257–64.
7. Alp E. Risk factors for nosocomial infection and mortality in burn patients: 10 years of experience at a university hospital. J. Burn Care Res. 2012;33(3):379–85
8. Sherren PB, Hussey J, Martin R, Kundishora T. Lethal triad in severe burns. Burns. 2014;40(8):1492–6.
9. Lu RP, Ni A, Lin FC, Ortiz-Pujols SM, Adams SD, Monroe DM 3rd, Whinna HC, Cairns BA, Key NS. Major burn injury is not associated with acute traumatic coagulopathy. J Trauma Acute Care Surg. 2013;74(6):1474–9. doi: 10.1097/TA.0b013e3182923193
10. Ronco C, Bellomo R, Homel P, Brendolan A, Dan M, P Piccinni P, La Greca G. Effects of different doses in continuous veno-venous haemofiltration on outcomes of acute renal failure: a prospective randomised trial. Lancet. 2000;356(9223):26–30. doi: 10.1016/S0140-6736(00)02430-2
11. Borthwick EM, Hill CJ, Rabindranath KS, Maxwell AP, McAuley DF, Blackwood B. High-volume haemofiltration for sepsis in adults. The Cochrane database of systematic reviews. 2017;1:1–39. doi: 10.1002/14651858
12. Chung KK, Coates EC, Smith DJ Jr, Karlnoski RA, Hickerson WL, et al. Randomized controlled Evaluation of high-volume hemofiltration in adult burn patients with Septic shoCk and acUte kidnEy injury (RESCUE) Investigators. High-volume hemofiltration in adult burn patients with septic shock and acute kidney injury: a multicenter randomized controlled trial. Crit Care. 2017;21(1):289. doi: 10.1186/s13054-017-1878-8
Об авторах
П. А. ГрибаньРоссия
Грибань Павел Андреевич – канд. мед. наук, врач-хирург; доцент института хирургии
690002, г. Владивосток, пр-т Острякова, 2
К. В. Майстровский
Россия
В. В. Усов
Россия
О. Е. Оробий
Россия
А. А. Полежаев
Россия
Т. Н. Обыденникова
Россия
С. М. Терехов
Россия
Е. Е. Костива
Россия
Рецензия
Для цитирования:
Грибань П.А., Майстровский К.В., Усов В.В., Оробий О.Е., Полежаев А.А., Обыденникова Т.Н., Терехов С.М., Костива Е.Е. Опыт применения продленной вено-венозной гемодиафильтрации в интенсивной терапии пациентов с тяжелой термической травмой. Тихоокеанский медицинский журнал. 2025;(2):86-91. https://doi.org/10.34215/1609-1175-2025-2-86-91
For citation:
Griban P.A., Maystrovskiy K.V., Usov V.V., Orobiy O.E., Polezhaev A.A., Obydennikova T.N., Terehov S.M., Kostiva E.E. Application of prolonged veno-venous hemodiafiltration in intensive care for patients with severe thermal injuries. Pacific Medical Journal. 2025;(2):86-91. (In Russ.) https://doi.org/10.34215/1609-1175-2025-2-86-91





































